1. Anatomie der Hypophyse
2. Physiologie
Regelkreise
3. Symptome
4. Radiologische Diagnostik
5. Therapie
6. postoperative Nachsorge
Antworten auf Fragen
|
Größe: |
ca. 1 - 1,5 cm Durchmesser
 |
|
Gewicht: |
0,5 - 0,6 gr
 |
|
Lage: |
in der Sella turcica, über den Hypophysenstiel verbunden mit dem
Hypothalamus.
(siehe Bild im Anhang) |
Die Hypophyse setzt sich zusammen aus:
a) Adenohypophyse (= Hormondrüse, produziert also selbst Hormone)
b) Neurohypophyse (leitet Hormone aus dem Hlypothalamus weiter = Oxytocin und
ADH)

Die Hypophyse ist übergeordnete Hormondrüse für:
> Geschlechtsorgane
> Schilddrüse
> Nebennierenrinde
Direkte Beeinflussung von:
> Körpergröße
> Wasserhaushalt
Der Hypothalamus schickt bis auf zwei Ausnahmen (Oxytocin und ADH) sogenannte ,,Releasing Hormone" an die Adenohypophyse, wo diese entsprechende Hypophysen
Hormone freisetzen. Bestimmte Rezeptoren in den Erfolgsorganen leiten den Sättigungsgrad der jeweiligen Hormone an den Hypothalamus weiter, der somit seine
Ausschüttung von Releasing Hormonen regeln kann, über die sogenannten Regelkreise.
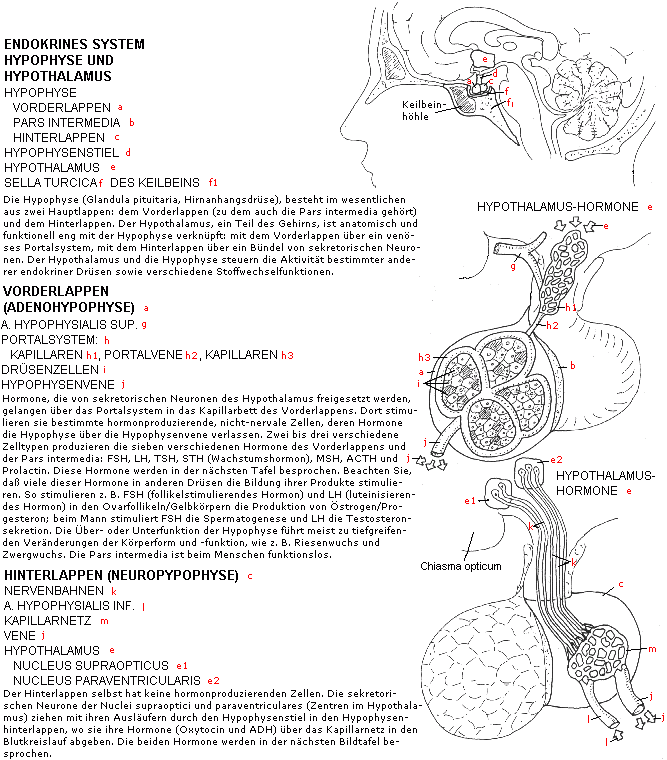

Hormonale Regelkreise
|
W W W W W W W W W W W W W W W W W W W
W W W W W W W W W W |
aus s
R.F. Schmidt G.Thews (Hrsg.)
Physiologie des Menschen
23. Auflage
Springer Verlag
Seitenanfang
|
|
|
|
Hypophysenvorderlappenhormone |
Kurzbe-
zeichnung |
Name |
Wirkung auf |
| Glandotrope Hormone |
| ACTH |
Adrenocorticotropes Hormon
(syn. Corticotropin) |
Nebennieren-
rinde |
| TSH |
Thyreoidea-stimulierendes-Hormon |
Schilddrüse |
| FSH |
Follikel-stimulierendes-Hormon |
Gonaden |
| LH |
Luteinisierendes-Hormon |
Gonaden |
| Nicht-glandotrope Hormone |
| GH |
Wachstumshormon
(engl. Growth Hormon)
(syn. Somatotropes Hormon=STH) |
Alle Körper-
zellen |
| |
Prolactin |
Viele Körper-
zellen
(Mamma,
Gonaden) |
|
i
|
| Releasing- und
Inhibitinghormone |
Kurzbe-
zeichnug |
Name |
Wirkung auf |
| Releasinghormone |
| TRH |
Thyreotropin-Releasing-Hormon |
TSH |
| LHRH |
Luteinisierendes Hormon
Releasing-Hormon
(syn. GnRH |
LH und
FSH |
| CRH |
Corticotropin-Releasing-Hormon |
ACTH |
| GHRH |
Growth Hormone-Releasing
Hormon |
PRL |
| PRH |
Prolactin Releasing-Hormon |
PRL |
| Inhibitinghormone |
| GHIH |
Growth Hormone-Inhibiting-
Hormon
(syn. Somatostatin, SS) |
GH |
| PIH |
Prolactin-Inhibiting-Hormon |
PRL |
|
|
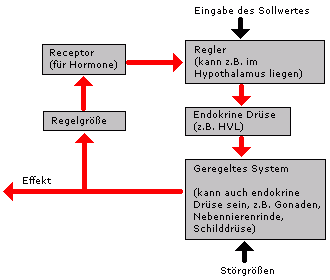
Schematische Darstellung eines Regelkreises für endokrine Regulationen. Die Eingabe eines Sollwertes für die Führungsgröße erfolgt durch einen Regler,
der die endokrine Drüse steuert. Die endokrine Drüse sezerniert Hormone. Diese Sekretion kann durch Störgrößen verändert werden. Hormone regeln dann ein System,
das auf die hormonelle Nachricht reagiert. Daraus resultiert ein physiologischer Effekt. Gleichzeitig wird die Regelgröße über Rezeptoren dem Regler mitgeteilt und der
Regelkreis so geschlossen.
|
|
|
|
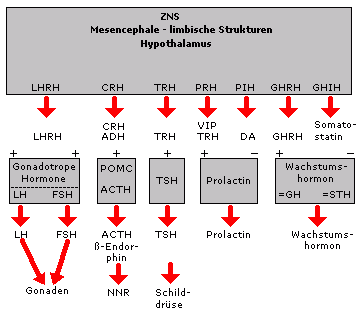
Grundprinzipien der Regulation von Hypophysenvorderlappenhormonen (untere Kästen) durch den Hypothalamus (oberer Kasten). Zur Nomenklatur
siehe Tabellen oben. Die 4 glandotropen Hormone LH, FSH, ACTH und TSH haben jeweils nur ein Zielorgan im Körper. Dieses ist eine Drüse. Die beiden anderen Hormone (Prolactin und Wachstumshormon) wirken an den Zellen vieler Organe. Zur Bedeutung der Proopiomelanocortinzelle POMC im Zusammenhang mit der ACTH-produzierenden Zelle
siehe Fachliteratur. Alle Hormone des Hypophysenvorderlappens werden durch hypothalamische Neurohormone reguliert.
|
|
|
|
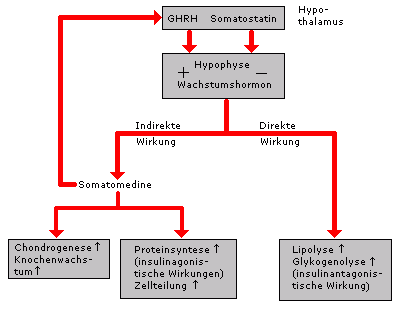
Regulation des Wachstumshormons durch GHRH und Somatostatin und Hormonwirkungen. Das Wachstumshormon wirkt direkt auf die Lipolyse und die Glykogenolyse und stimuliert in der Leber die Bildung von Somatomedinen. Diese Somatomedine koppeln zum Hypothalamus zurück und schließen so einen Regelkreis. Im Körper stimulieren sie die Chondrogenese und das Knochenwachstum sowie die Proteinsynthese und die Zellteilung.
|
|
|
|
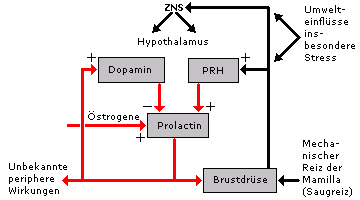
Regulation
des Prolactins. Im Hypothalamus liegen die sog. tuberoinfundibulären
dopaminergen (TIDA-) Zellen, welche ständig Dopamin als
Prolactin-Inhibiting-Hormon ausschütten. Prolactin koppelt
autoregulatorisch zu den TIDA-Neuronen zurück. Dieser Regelkreis kann
durch zahlreiche Umwelt- und Innenwelteinflüsse, die zur Ausschüttung
eines oder mehrerer Prolactin-Releasing-Hormone (PRH) führen, beeinflußt
werden. Hohe Östrogenspiegel stellen Innenwelteinflüsse mit
prolactinstimulierender Wirkung dar. Das übrige ZNS ist über limbische
und mesencephale Einflüsse auf PRH-Neurone und dopaminerge Zellen mit
an der Regulation der Prolactinsekretion beteiligt.
|
|
|
|
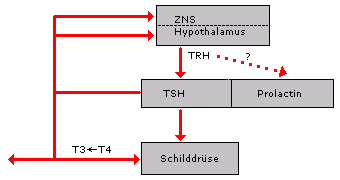
Hypothalamo-hypophysio-thyreoidaler Regelkreis. Hypothalamische Neurone produzieren das Thyreotropin-Releasing-Hormon (TRH). Dieses gelangt über die portalen Gefäße zur Hypophyse und regt dort die Sekretion des Thyreoidea-stimulierenden Hormons (TSH) an. TSH bewirkt in der Schilddrüse die Produktion von Thyroxin und Trijodthyronin.
T3 koppelt zur Hypophyse, in untergeordnetem Maße wohl auch zum Hypothalamus zurück, so daß die TSH-Sekretion ausbalanciert ist. Ob das vom Hypothalamus ausgeschüttete TRH auch unter physiologischen Bedingungen die Prolactinsekretion stimuliert, ist unklar.
|
|
|
|
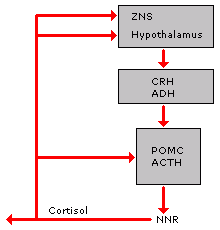
Hypothalamo-hypophysio-adrenaler Regelkreis. Neurone des Hypothalamus produzieren das Corticotropin-Releasing-Hormon (CRH). Dieses gelangt über die portalen Gefäße zur Hypophyse und stimuliert hier die ACTH-Sekretion. ACTH bewirkt an den Nebennieren vermehrte Cortisolsynthese und -ausschüttung. Das Cortisol koppelt sowohl zur Hypophyse als auch zum Hypothalamus zurück. Dieses geregelte System wird leicht durch Umwelteinflüsse (insbesondere diverse Stressoren) aus dem Gleichgewicht gebracht. Ob das antidiuretische Hormon (ADH) unter physiologischen Bedingungen als ein zusätzliches CRH angesehen werden muß, ist z.Z. noch nicht geklärt. Über suprahypothalamische, insbesondere mesencephale und limbische Einflüsse können Informationen über Emotionen, Schmerz etc. an die hypothalamischen ACTH-produzierenden Zellen übertragen werden.
|
|
w w w w w w w w w w w w w w w w w w w w w w w w w w
w w w w w w w w w w w w w w w w w w w w w w w w w w w w w w w w w w
w w w w w w w w w w w w w w w w w w w w w w w w
|
aus
R.F. Schmidt G.Thews (Hrsg.)
Physiologie des Menschen
23. Auflage
Springer Verlag
|
|
|
|
Seitenanfang |
|
|
a) der globalen Unterfunktion (bei hormoninaktiven Adenomen, sie machen ca. 33% der Hypophysenadenome aus):
- fahlgelbes Hautkolorit
- Rückgang der Geschlechtsbehaarung
- Hypogonadismus
- Oligomenorrhoe, Amenorrhoe Libidoverlust
- Verlust der lateralen Augenbrauen
- Adynamie (Schwäche, Kraftlosigkeit)
- Hypotonie
- Obstipation
- Kälteempfindlichkeit
- Diabetes insipidus
- Kleinwuchs (bei Kindern)
Ältere Patienten merken oft nicht, daß die Symptome von der Hypophyse kommen, deswegen wird die Diagnose meist erst nach Auftreten zusätzlicher Sehstörungen gemacht.
b) der spezifischen Überfunktion bei Prolaktinomen, bei ACTH produzierenden Adenomen (M. Cushing), bei STH produzierenden Adenomen (Akromegalie):
Prolaktinome (ca. 30% der Hypophysenadenome)
|
Symptome bei Frauen: |
- unregelmäßige Menstruation |
|
- Oligomenorrhoe, Amenorrhoe |
|
- Galaktorrhoe (spontane milchige Absonderungen aus der Brustdrüse außerhalb der
Laktationsperiode)
 |
|
bei Männern: |
- Libidoverlust |
|
- Potenzstörungen |
|
- Gynäkomastie |
|
>häufig späte Diagnose bei Männern |
Diagnostik: Hyperprolaktinämie im Serum (z.T. ist das Prolaktin um das hundertfache erhöht)
ACTH produzierende Adenome (ca. 10 - 15 % aller
Hypophysenadenome)
Symptome (M.Cushing):
- Fettstoffwechselstörungen ( Stammfettsucht, Striae, Hypercholesterinämie)
- Eiweißstoffwechselstörung ( Osteoporose, Muskelschwund, Adynamie)
- Kohlenhydratstoffwechselstörung ( Diabetes mellitus)
- Hypertonie (mineralkortikoide Wirkung)
- Akne, Ulcera
- psychische Störungen ( Depressionen, Psychosen)
Diagnostik:
- aufgehobene Tagesrhythmik!
- ACTH im Serum erhöht
- ACTH durch CRH überschießend stimulierbar
- Dexamethason Hemmtest
STH produzierende Adenome (ca.20% aller Hypophysenadenome)
Symptome:
- Akromegalie Füße, Hände, Kinn, Orbitawulst)
- Visceromegalie (Kardiomegalie, Herzinsuffizienz)
- Hirsutismus (Bartwuchs bei Frauen)
- Hyperhidrosis (Steigerung der Schweißsekretion)
- Diabetes mellitus
- Riesenwuchs (bei Kindern)
Diagnostik:
- STH Bestimmung im Serum
- oraler Glucose-Toleranz-Test (durch Zucker geht STH normalerweise runter)
c) Sehstörungen
> Hemianopsie - Gesichtsfeldeinschränkung
durch Druck des Tumors z.B. auf das Chiasma opticum (Sehnervenkreuzung)

MRT, CT
Nachweis intrasellärer Adenome ab einer Größe von etwa 5 mm. Mikroadenome zeigen gegenüber dem gesunden Hypophysengewebe eine zeitlich verzögerte,
oder eine geringere Kontrastmittelanreicherung, d.h. das KM geht überwiegend in die Hypophyse, nicht in das Adenom.
Schädelübersicht
- Aufweitung der Sella
- Doppelkonturierung
- Ausdünnung des Sellabodens
Angiographie
- Spreizung und Verlagerung des Carotissiphons
- Anhebung der Arteria cerebri anterior
- Zum Ausschluß von Carotis-Aneurysmen (die z.T. aussehen wie
Hypophysenadenome)
i.d.R. ist die Angio verzichtbar und es reicht ein MRT-Angio aus.
a) medikamentös:
bei Prolaktinomen mit Bromocriptin (Pravidel) wenn
- keine Sehstörungen vorliegen
- der Tumor kleiner als ca. 1 cm ist
- der basale Prolaktinspiegel < 500 u/ml ist
- keine weiteren Hormonstörungen vorliegen
Normalisierungsrate bei kleinen Prolaktinomen etwa 70 %.
Pravidel kann zu Komplikationen in der Schwangerschaft führen, deswegen sollten bei Kinderwunsch auch kleine Prolaktinome operiert werden.
b) operative Therapie:
bei überwiegend intrasellär gelegenen Adenomen: transphenoidaler Zugang (erstmals 1914 von H. Cushing detailliert beschrieben)
bei überwiegend suprasellär gelegenen Adenomen: pterionaler/subfrontaler Zugang
(Kraniotomie)
Die Hypophyse wird in der Regel ganz entfernt, da eine Unterscheidung zwischen Hypophyse und Adenom kaum möglich ist (dadurch lebenslange Hormonsubstitution nötig).
Evtl. intraoperatives Hormonmonitoring : während der OP wird der Hormonspiegel abgenommen und ausgewertet. Es wird dann so lange nach dem Adenom gesucht,
bis der Prolaktinspiegel runter gegangen ist.
Perioperative Gabe von 200 mg Hydrocortison i.v., da trotz erhöhtem Streß kein eigenes Kortison produziert wird.
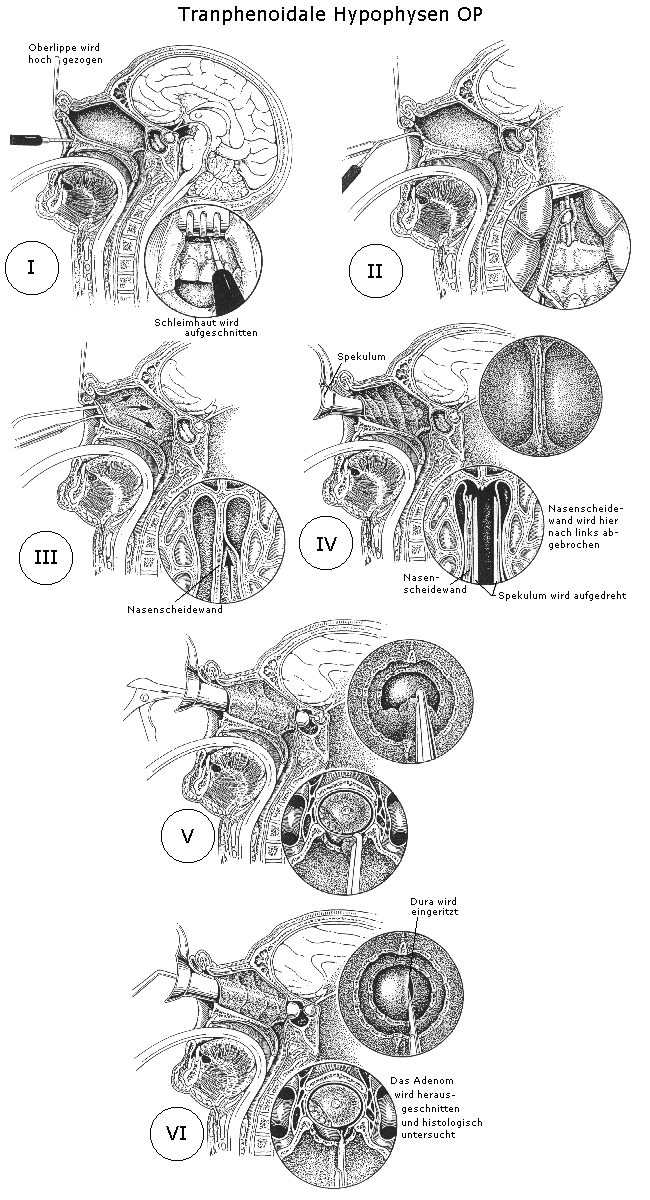
a) Nasentamponade für 4-5 Tage, hält hauptsächlich die gebrochene Nasenscheidewand in der Mitte und saugt Wundflüssigkeit auf
b) Hormonsubstitution
|
Hydrocortison: |
zunächst 2OOmg i.v., dann schrittweise reduzieren.
Erhaltungsdosis 3Omg/d
Achtung: Tagesrhythmik
Dosiserhöhung bei Fieber, Streß (Schmerzen)
 |
| T3/T4: |
täglich 75-125ug L-Thyroxin
 |
| Geschlechtshormone: |
z.B. Primobolan depot |
c) Überwachung wegen möglichem Diabetes insipidus (ADH - Mangel)
- Ausscheiden großer Mengen nicht konzentrierten Urins
 Urinosm9larität niedrig Urinosm9larität niedrig
 Urin-Natrium-Konzentration niedrig Urin-Natrium-Konzentration niedrig
 Urinmenge hoch Urinmenge hoch
 viel Durst viel Durst
Therapie: Minirin s.c. oder als Nasenspray.
| - |
Entnahme von Bauchfett: manche Operateure nehmen das Fett als "Fett-Plombe" z.B. in der Keilbeinhöhle zum Abdichten von
Liquorfisteln Die Maßnahme ist aber umstritten, da sie evtl. zu Nekrose führen kann.
 |
| - |
Manchmal wird Luft in den Kopf gepumpt, das ergibt klarere Konturen auf dem Röntgenbild, außerdem soll das Adenom
nach unten gedrückt werden, daß der Operateur besser dran kommt.
 |
| - |
Adenome machen ca. 10% aller Hirntumore aus Adeno-Carzinom ist sehr selten
 |
| - |
Patient braucht lebenslange Hormonsubstitution
 |
| - |
ADH wird durch den Hypothalamus auch nach einer Hypophysen-OP wieder ausgeschieden, deswegen muß der Patient
sehen ein Leben lang Minirin nehmen
 |
| - |
Nur in Ausnahmefällen muß bestrahlt werden, falls sich noch Reste im Kopf befinden
 |
| - |
Komplikationsrate etwa 5 % |
- Infektionen
- Gefäßverletzung (Carotis)
- Rhinoliquorrhoe |
Anhang
C) Auszug aus dem Krankenpflegeunterricht ,Innere Medizin' von Frau Dr. Zopf über Hormone und Krankheitsbilder betreffend Hypophyse und Hypothalamus
|










